قررت وزارة الصحة سحب مشغل وعقار زانتاك بجميع أشكاله وتركيزاته من السوق المصري، ووقف تداول جميع الأشكال الصيدلانية المحتوية على مادة الرانيتيدين، بناء على تقرير منظمة الصحة العالمية باحتمالية وجود شوائب مسرطنة في هذه المادة.
وأعلنت وزرة الصحة ممثلة في الإدارة المركزية للشئون الصيدلية، في منشور رسمي، سحب مشغل وعقار زانتاك بجميع أشكاله وتركيزاته من السوق الدوائي، ووقف تداول جميع الأشكال الصيدلانية المحتوية على مادة الرانيتيدين.
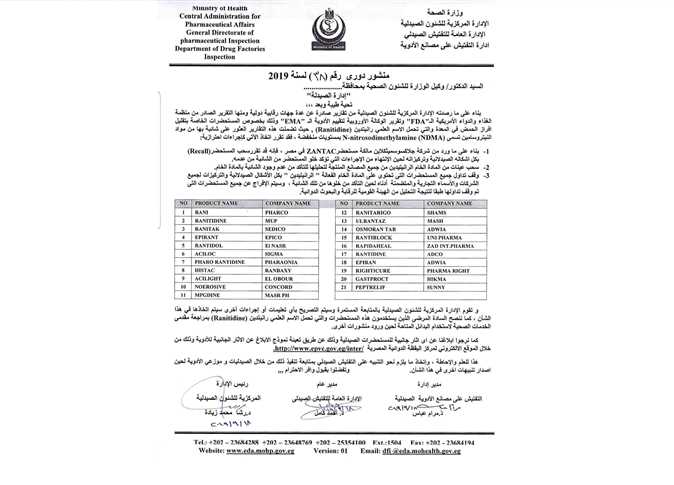
سحب مشغل وعقار زانتاك
وحمل المنشور رقم 38 لعام 2019، وتضمن مخاطبة الشركة المنتجة، لسحب كل التشغيلات من السوق لحين ثبوت عدم احتوائها على شوائب مسرطنة.
وجاء قرار سحب مشغل وعقار زانتاك بناء على تأكيد إدارة الغذاء والدواء الأمريكية أن بعض الأدوية التي يحتوي على مادة الرانيتيدين، بما في ذلك الدواء الذي يحمل الاسم التجاري Zantac، يحتوي على شوائب نيتروسامين، تسمى Nnitrosodimethylamine NDMA بمستويات منخفضة، إذ يُجرى تصنيف NDMA كمادة مسرطنة محتملة للإنسان، بناء على نتائج الاختبارات المعملية.
وتُعد شوائب NDMA من الملوثات البيئية المعروفة، وتوجد في الماء والأطعمة، بما في ذلك اللحوم ومنتجات الألبان والخضراوات.
وتقوم إدارة الأغذية والعقاقير (FDA) بالتحقيق في NDMA وغيرها من شوائب النتروزامين في أدوية ضغط الدم، وفشل القلب، التي تسمى حاصرات مستقبلات Angiotensin II ARBs منذ العام الماضي، في حالة ARBs.
وأوصت إدارة الأغذية والعقاقير بالعديد من عمليات الاسترجاع، المتمثلة في سحب مشغل وعقار زانتاك المحتوية عليها، لأنها اكتشفت مستويات غير مقبولة من النتروزامين.
ومن المؤكد أن شوائب NDMA قد تتسبب في ضرر حال وجودها بكميات كبيرة، إلا أن المستويات التي كشفت عنها الاختبارات الأولية التي أجرتها FDA في رانيتيدين بالكاد تتجاوز الكميات التي قد تتوقع العثور عليها في الأطعمة الشائعة.
مادة الرانتيدين
ورغم تأكيدها على سحب مشغل وعقار زانتاك المُحتوِي على الرانتيدين، فإن إدارة الأغذية والعقاقير ما زالت تقيم ما إذا كانت المستويات المنخفضة من NDMA في الرانيتيدين تشكل خطرا على المرضى أم لا.
وأوضحت إدارة الأغذية والعقاقير أنها لا تدعو الأفراد للتوقف عن تناول رانيتيدين في هذا الوقت، ومع ذلك يجب على المرضى الذين يتناولونه بوصفة طبية ويرغبون في التوقف عن الاستخدام التحدث إلى اختصاصي الرعاية الصحية لديهم، بشأن خيارات العلاج الأخرى.
وأهابت بأنه يجب على المستهلكين ومختصي الرعاية الصحية الإبلاغ عن أي ردود فعل سلبية مع رانيتيدين على برنامج MedWatch التابع لإدارة الأغذية والعقاقير، لمساعدة الوكالة في فهم نطاق المشكلة بشكل أفضل.
وتستخدم مادة رانيتيدين لعلاج الحموضة، وهي عبارة عن مانع H2 (الهيستامين -2) ما يقلل من كمية الحمض الناتجة عن المعدة.
وجرت الموافقة على استخدام الرانيتيدين دون وصفة طبية، لمنع وتخفيف حرقة المعدة المرتبطة بتناول الحمض والمعدة الحامضة.










أضف تعليق